Sistema de Gestión de Calidad de Halco
Halco se compromete a mantener y mejorar continuamente la calidad de nuestros métodos de producción y de los proyectos de conversión de gancho y bucle gestionados en nombre de nuestros clientes. Los requisitos específicos del cliente, los requisitos reglamentarios aplicables, el seguimiento y la medición, los procedimientos, la gestión de riesgos y la excelente documentación técnica son parte esencial de nuestro sistema de gestión de calidad.
Los procesos de calidad de Halco ya cumplieron o superaron los requisitos de ISO 9001 2015 y, nos complace anunciar, ahora cumple con los criterios de aceptación para recibir la certificación ISO 13485 2016 para la fabricación de dispositivos médicos. Halco no fabrica dispositivos médicos terminados, pero sí proporcionamos servicios de conversión personalizados de alta calidad para la fabricación de componentes de dispositivos médicos utilizando nuestros sujetadores de gancho y bucle y otros materiales flexibles. Esto demuestra que Halco demostrará consistentemente el cumplimiento de las expectativas de calidad del cliente, las regulaciones relevantes y las especificaciones de dispositivos médicos.

James Fussell, jefe de Calidad e Ingeniería de Halco, comenta:
"Nuestra reciente acreditación ISO13485 nos coloca en una posición única como proveedor y convertidor líder de sujetadores de gancho y bucle. Para nuestros clientes médicos, poder redactar SOP de acuerdo con los requisitos 13485 nos coloca en una posición sólida no solo para ofrecer un producto certificado, sino también para implementar controles de proceso que sabemos que cumplen con las especificaciones ISO y del cliente."
¿Qué es ISO 13485 y cuáles son sus requisitos?
ISO 13485 2016 es un conjunto de requisitos y estándares para los fabricantes de dispositivos médicos y sus proveedores, en cualquier etapa del ciclo de vida, para demostrar que pueden cumplir consistentemente con los requisitos regulatorios relevantes y de los clientes.
ISO 13485 2016 tiene ocho secciones diferentes. Las primeras tres secciones, o “cláusulas”, son introductorias y las cinco últimas definen lo que se requiere.
- Cláusula 4. Esta sección cubre los requisitos generales de los sistemas de gestión de calidad (QMS) y los requisitos de documentación. En la sección del SGC, el principio básico es que la organización hace lo que dice que va a hacer desde una perspectiva de gestión de la calidad y que se adhiere a los principios de una buena organización de gestión de la calidad. En los requisitos de documentación, el elemento crítico es la creación de un “archivo de dispositivo médico”para cada dispositivo y un plan de control para la gestión y retención de ese archivo.
- Cláusulas 5-8. Estas secciones tratan los temas de responsabilidad de gestión, sistemas de gestión de recursos, los procesos de realización de productos que van desde la conceptualización hasta la implementación y, finalmente, cómo una organización realiza mediciones, análisis y mejoras.
¿Qué es un expediente de dispositivo médico?
La norma ISO 13485 2016 exige la creación de un archivo de dispositivo médico que almacene exhaustivamente todos los documentos de cada dispositivo médico o familia de dispositivos médicos. Este archivo contiene todos los documentos que describen el diseño de productoespecificaciones del producto, procesos de fabricación y ensamblaje, uso de dispositivos médicos, monitoreo y medición de calidad, cumplimiento normativo y estándares de calidad. Si corresponde, el archivo también contendrá registros y documentación relacionados con servicios, mantenimiento e instalación. Finalmente, se creará un plan de control claro para controlar, proteger y conservar el archivo.
¿Cuál es la diferencia entre ISO 9001 e ISO 13485?
La norma ISO 9001 2015 y la ISO 13485 2016 tienen muchas similitudes. Sin embargo, la norma 13485 se desarrolló a partir de la norma ISO 9001 2008. Existen una gama de diferencias que son específicos de la industria de dispositivos médicos. Muchos anticipan que los requisitos de la norma 13485 se actualizarán para alinearse más con la norma ISO 9001 2016.

¿Cuál es el beneficio para los clientes médicos de Halco?
Halco ya es un proveedor certificado ISO de alta calidad y confiable para muchos fabricantes de dispositivos médicos. Con la certificación ISO 13485, los OEM de dispositivos médicos pueden confiar y comunicarse con confianza en que Halco fabrica y suministra componentes de fijación de gancho y bucle convertidos que cumplen con los requisitos reglamentarios y de calidad de ISO 13485 2016 y los requisitos de sus clientes.
¿Qué puede esperar del futuro de Halco?
Halco continúa invirtiendo en el desarrollo de productos y capacidades de troquelado para la fabricación de dispositivos médicos. Nuestra experiencia en segmentos como vestibles, posicionamiento de pacientes, fabricación de batas y paños, apnea del sueño y fijación de tubos con sujetadores que se pueden volver a cerrar adecuados para estas aplicaciones son insuperables. Durante 2023, Halco espera el lanzamiento de nuevos productos, incluidos adhesivos especiales, y una importante inversión en equipos para mantenerse a la vanguardia de la industria de fijaciones de gancho y bucle.
Para obtener más información sobre los productos de Halco para la industria de dispositivos médicos, visítenos aqui. Halco también proporciona muestras para evaluación de su diseño y se especializa en servicios de conversión de alto rendimiento para componentes de fijación de gancho y bucle.
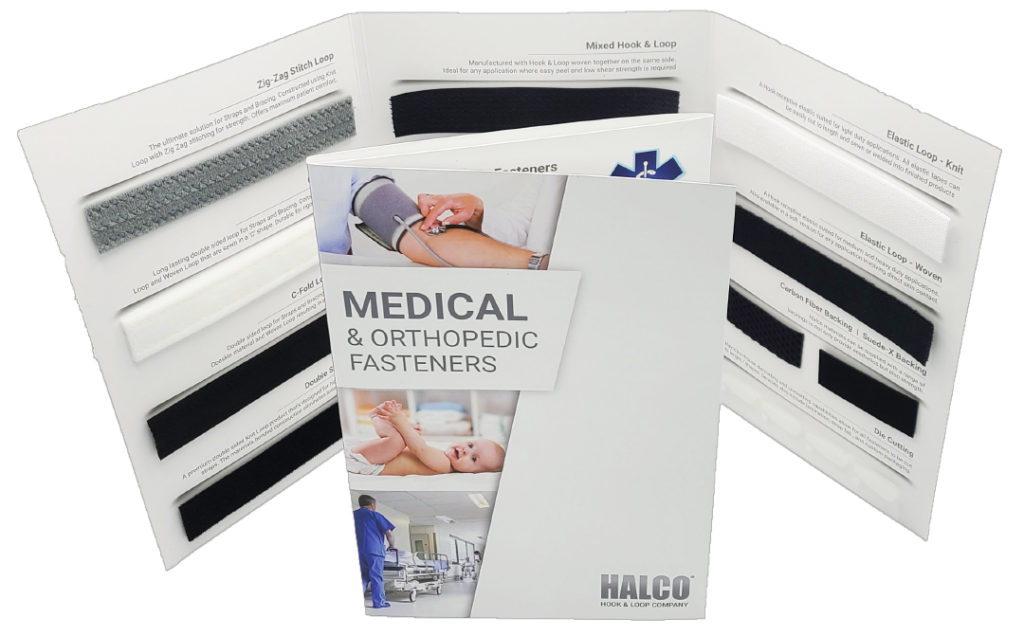
¡Cuéntenos un poco más sobre su proyecto y solicite nuestro kit de muestra de gancho y bucle para dispositivos médicos!